高效液相色谱方法的建立 01:分析方法开发
HPLC 方法建立步骤
graph LR 1-1[有关样品的情况,明确分离目的] --> 2-1[是否需要特殊的 HPLC 步骤、样品预处理等?] --> 3-1[选择检测器和检测器设备] --> 4-1[选择液相色谱法,进行预试验,估计最佳分离条件] --> 5-1[优化分离条件] --> 6-1[检查出现的问题或所需的特殊步骤] --> 7-1[论证方法使之进入常规实验室]
良好的系统适用性参数
一个好的分析方法,应该尽量满足:
- 目标峰分离度足够高(\(R_s \geq 2\));
- 保留因子 \(1<k<10\);
- 总的分析时间 \(t_{Total} \leq 20\) min;
- 拖尾因子 \(T_f \to 1\) 且 \(T_f<2\);
- 进样重现性(如:RSD 0.1%–0.25%);
- 信噪比:\(S/N>10\)。
分离度
HPLC 法的基本条件应达到多组分的相互分离。根据分离度的定义式:
\[ R_{s} = \frac{2(t_{R2} - t_{R1})}{W_1 + W_2} \]
可知要分离得好,有两条途径:一是谱带窄,即柱效高;再就是谱带间距离大。
Purnell 方程
分离度 \(R_s\) 也用 Purnell 方程表示:
\[ R_s = \frac{\sqrt{N_2}}{4} \cdot \frac{(\alpha - 1)}{\alpha} \cdot \frac{k_2}{(k_2+1)} \]
假设 \(W_1 \approx W_2\),可以在数学上证明:
\[ R_s = \frac{2(t_{R2}-t_{R1})}{W_1 + W_2} = \frac{\sqrt{N_2}}{4} \cdot \frac{(\alpha - 1)}{\alpha} \cdot \frac{k_2}{(k_2+1)} \]
具体证明如下:
\[ \begin{align*} R_s &= \frac{\sqrt{N}}{4} \cdot \frac{(\alpha - 1)}{\alpha} \cdot \frac{k_2}{(k_2+1)} \\ &=\frac{\sqrt{16 \left( \frac{t_{R2}}{W_2} \right)^2}}{4} \cdot \frac{\frac{k_2}{k_1}-1}{\frac{k_2}{k_1}} \cdot \frac{k_2}{k_2+1}\\ &=\frac{t_{R2}}{W_2} \cdot \frac{k_2-k_1}{k_2} \cdot \frac{k_2}{k_2+1}\\ &=\frac{t_{R2}}{W_2} \cdot \frac{k_2-k_1}{k_2+1}\\ &=\frac{t_{R2}}{W_2} \cdot \frac{\frac{t_{R2}-t_{0}}{t_{0}}-\frac{t_{R1}-t_{0}}{t_{0}}}{\frac{t_{R2}-t_{0}}{t_{0}}+1}\\ &=\frac{t_{R2}}{W_2} \cdot \frac{t_{R2}-t_{R1}}{t_{R2}}\\ &=\frac{t_{R2}-t_{R1}}{W_2}\\ \end{align*} \]
假设 \(W_1 \approx W_2\),有:
\[ \begin{align*} R_s &= \frac{\sqrt{N_2}}{4} \cdot \frac{(\alpha - 1)}{\alpha} \cdot \frac{k_2}{(k_2+1)} \\ &=\frac{t_{R2}-t_{R1}}{W_2}\\ &=\frac{2(t_{R2}-t_{R1})}{W_1 + W_2}\\ \end{align*} \] 得证。
Purnell 方程也直接写成:
\[ R_s = \frac{2(t_{R2}-t_{R1})}{W_1 + W_2} = \frac{\sqrt{N}}{4} \cdot \frac{(\alpha - 1)}{\alpha} \cdot \frac{k}{(k+1)} \]
- 保留值(Rention):\(k\)
- 选择性(Selectivity):\(\alpha\)
- 柱效(Efficiency):\(N\)
将上述三项看作相互独立的参数,可以简化条件优化步骤。
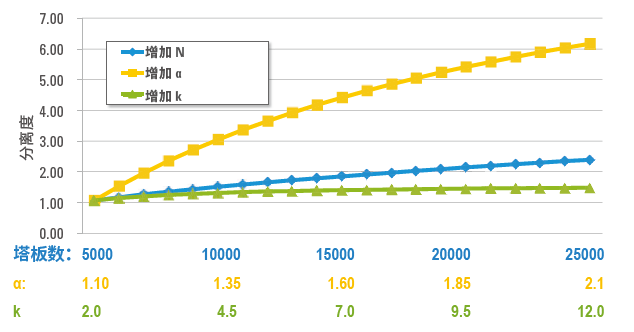
Figure 1. 保留因子(\(k\))、选择性(\(\alpha\))和塔板数(\(N\))对分离度的影响
由上图可知,对分离度影响程度 \(\alpha > N > k\)。\(\alpha\) 项(即选择性)对分离度的影响远大于柱效和保留因子。因此,在方法开发过程中,改变选择性将对实现分离所需的分离度产生最大影响。
影响分离度的条件
Table 1. 不同的分离条件对保留因子(\(k\))、选择性(\(\alpha\))和塔板数(\(N\))的影响
| 条件 | \(k\) | \(\alpha\) | \(N\) |
|---|---|---|---|
| 流动相的 pHa | ++ | ++ | + |
| 离子对试剂浓度a, b | ++ | ++ | + |
| 色谱柱类型(C18、苯基、氰基等) | + | ++ | - |
| B 溶剂(乙腈、甲醇等) | + | ++ | - |
| %B | ++ | + | - |
| 温度 | + | + | + |
| 缓冲液浓度a | + | + | - |
| 柱长 | 0 | 0 | ++ |
| 粒径 | 0 | 0 | ++ |
| 流速 | 0 | 0 | + |
| 柱压 | - | - | +c |
注:++:主要影响;+:次要影响;-:相对影响很小;0:没有影响;加粗的量主要(和推荐)用于分别控制 \(k\)、\(\alpha\) 和 \(N\)。
a:适用于可电离的溶质分子(酸或碱)来说;
b:在离子对色谱中尤其重要;
c:通过适当选择其他分离条件,压力较高时,\(N\) 值也较高;然而压力本身对 \(N\) 的直接影响可以忽略不计。
pH 的影响
当分析物含有可电离官能团时,处于离子状态时的极性大,因此想要化合物在反相色谱上有更好的保留,化合物应该尽量不电离。
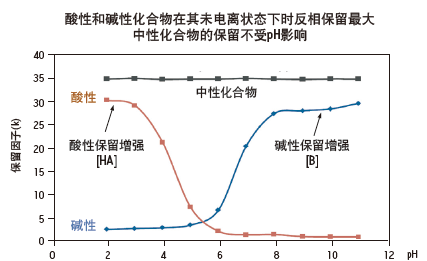
Figure 2. pH 对化合物保留的影响
对于酸性化合物
\[ \text{酸: }\mathrm{HA} \rightleftharpoons \mathrm{A}^{-} + \mathrm{H}^{+} \]
其电离常数
\[ K_a=\frac{[H^+][A^-]}{[HA]} \]
有
\[ pK_a=-\log_{10}K_{a} \]
对于碱性化合物
\[ \text{碱: }\mathrm{B} + \mathrm{H_{2}O} \rightleftharpoons \mathrm{BH}^{+} + \mathrm{OH}^{-} \]
其电离常数
\[ K_b=\frac{[BH^+][OH^-]}{[B]} \]
碱性化合物的 \(K_a\) 是其共轭酸的 \(K_a\),即 \(K_a=\frac{[B][H^+]}{[BH^+]}\),共轭酸碱对的电离常数乘积等于水的离子积常数(\(K_w\)):
\[ K_a\cdot K_b=K_w=1.0\times10^{-14} \]
因此碱性化合物
\[ pK_a=14-pK_b \]
根据 \(\text{pK}_a\) 定义式,不难推导:当 \(\text{pH} = \text{pK}_a\) 时,化合物一半处于电离,一半处于非电离状态。常将 pH 设置在 \(pK_a \pm 2\) 以上,此时 99% 以上的化合物将分别处于电离或未电离状态。
如何选择合适的 pH?
logP 是反映化合物脂溶性的参数,通常 logP 越大的化合物,其非极性越大,在反相色谱柱上的保留能力也就越强。logD 是描述化合物在不同 pH 条件下脂溶性的参数,对于非中性化合物来讲,其脂溶性会随着 pH 发生变化。
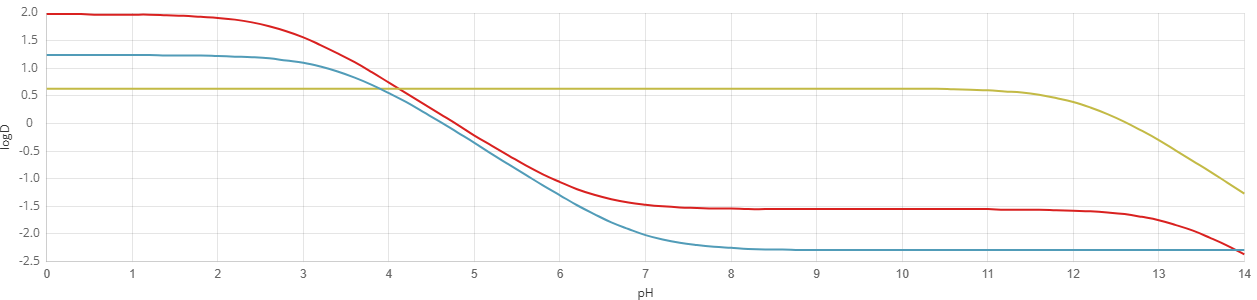
Figure 3. 某三种化合物的 logD-pH 关系图
上图是三种化合物的 logD-pH 关系图,可以看到在 \(pH \leq 2\) 时,三种化合物 logD 有较大的差异,有可能实现分离;且此时曲线也较为平缓,能够减少 pH 波动引起的重现性差。因此可以尝试设置 \(pH \leq 2\)。
Table 2. 常用的流动相 pH 调节剂
| 流动相化学成分 | pKa | 缓冲液范围 | 化学式 | 浓度为 10 mM 的流动相 (每 1 升) 所需的体积或质量 | pH 调节 酸/碱 | MS 兼容性 |
|---|---|---|---|---|---|---|
| 乙酸(冰醋酸) | 4.8 | – | CH3COOH | 0.571 mL | – | ✓ |
| 醋酸铵:pKa 1 | 4.8 | 3.8–5.8 | CH3COONH4 | 0.770 g | CH3COOH 或 NH4OH | ✓ |
| 醋酸铵:pKa 2 | 9.2 | 8.2–10.2 | CH3COONH4 | 0.770 g | CH3COOH 或 NH4OH | ✓ |
| 碳酸氢铵 | 9.2, 10.3 | (8.2–11.3) | NH4HCO3 | 0.790 g | HCOOH 或 NH4OH | ✓ |
| 碳酸铵 | 6.35, 9.25 | 5.9–6.9 和 8.8–9.8 | (NH4)2CO3 | 0.961 g | NH4OH | ✓ |
| 甲酸铵:pKa 1 | 3.8 | 2.8–4.8 | NH4COOH | 0.640 g | HCOOH 或 NH4OH | ✓ |
| 甲酸铵:pKa 2 | 9.2 | 8.2–10.2 | NH4COOH | 0.640 g | HCOOH 或 NH4OH | ✓ |
| 氨水 | 9.2 | – | NH4OH | 0.675 mL | – | ✓ |
| 磷酸氢二铵 | 7.2, 9.2 | (6.2–10.2) | (NH4)2HPO4 | 1.32 g | H3PO4 或 NH4OH | × |
| 甲酸 | 3.8 | – | HCOOH | 0.420 mL | – | ✓ |
| N-甲基吡咯烷 | 10.3 | – | C5H11NO | 1.04 mL | – | ✓ |
| 磷酸 | 2.1 | – | H3PO4 | 0.580 mL | – | × |
| 磷酸二氢钾 | 2.1 | (1.1–3.1) | KH2PO4 | 1.36 g | H3PO4 或 KOH | × |
| 磷酸氢二钾 | 7.2 | (6.2–8.2) | K2HPO4 | 1.74 g | H3PO4 或 KOH | × |
| 磷酸钾 | 12.7 | (11.7–13.7) | K3PO4 | 2.12 g | H3PO4 或 KOH | × |
| 吡咯烷 | 11.3 | – | C4H9N | 0.833 mL | – | ✓ |
| 硼酸钠 | 9.1, 12.7, 13.8 | (8.2–14) | Na2B4O7 | 2.01 g | H3BO3 或 NaOH | × |
| 柠檬酸三钠 | 3.1, 4.8, 6.4 | (2.1–7.4) | HOC(COONa)(CH2COONa)2 | 2.58 g | 柠檬酸或 NaOH | × |
| 三氟乙酸(TFA) | 0.3 | – | CF3COOH | 0.743 mL | – | × |
固定相的影响
固定相因其化学性质不同而会提供不同的保留与选择效果,色谱柱的选择可以参照“液相色谱柱”一文。
有机溶剂的影响
甲醇和乙腈,是用于反相色谱的典型有机溶剂。除了洗脱强度、粘度与柱背压有关、紫外吸收性不同,甲醇与乙腈在化学选择性上也有所不同,甲醇可以发生氢键作用,因此会提供显著不同的选择性。
甲醇
- 洗脱能力较弱。
- 质子化溶剂,提供氢键作用力,增强对化合物的洗脱能力,屏蔽硅醇基次级相互作用。
- 截止波长比乙腈大(205 nm)
乙腈
- 洗脱能力较强
- 非质子化溶剂
- 粘度较低(柱背压更低)
- 截止波长更短(190 nm)
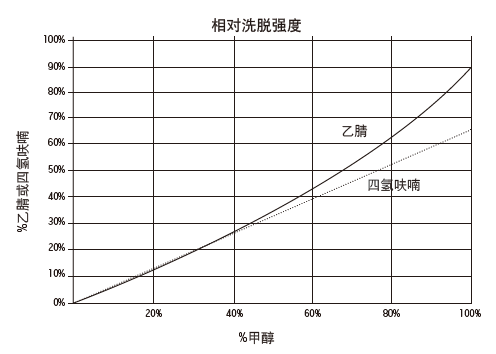
Figure 4. 有机溶剂相对洗脱强度曲线
梯度的影响
- 更缓的梯度可以提高分离度,色谱峰会展宽,导致灵敏度下降;
- 更陡的梯度斜率可能压缩色谱峰,灵敏度增加,经常会导致分离度的降低
改变梯度斜率时要平衡峰高与分离度的关系。
温度的影响
化合物保留随温度而变化的规律可以用下面这个等式描述:
\[ logk=A+B/T \]
- \(A, B\):对于给定的化合物是常数;
- \(T\):温度,单位 K。
因此温度的增加,会使化合物的保留 \(k\) 减小,引起选择性的改变(不一定是正向的);此外温度增加能减少流动相粘度,降低背压。
pH 调节剂的影响
“缓冲容量”是指 pH 调节剂维持恒定 pH 的能力,取决于以下几点考虑:
- pH 调节剂的 pKa 值;
- pH 调节剂的浓度;
- 流动相的 pH 值。
流动相的有效缓冲容量指的是当缓冲能力不足时,增加溶质的量并不会引起 pH 较大的变化。 以下的因素可以增加流动相的有效缓冲容量:
- 减少缓冲盐 pKa 值和流动相 pH 之间的差异(可调整 pH 或更换缓冲液)。
- 扩大流动相 pH 和溶质 pKa 值之间的差异(当差异足够大时,溶质被完全离子化或者保持非离子化形式,而此时,缓冲液就显得不重要了)。
- 增加缓冲液浓度。
- 减少样品进柱体积。
- 调节样品的 pH 与流动相的一致。
流动相的缓冲容量一般与缓冲液浓度成正比例关系,通常的浓度范围是 5–25 mM。
分析方法的建立
初始条件摸索
无论最终是采用等度洗脱还是梯度洗脱,都建议按照 Table 3 进行初始条件摸索。
Table 3. 初始条件参数
| 项目 | 类型 | 较好的初始条件 |
|---|---|---|
| 色谱柱a | ||
| 尺寸(长度 × 内径 ID) | 100 × 4.6 mm | |
| 粒度 | 3 μm | |
| 固定相 | C8 或 C18 | |
| 孔径 | 8–12 nm | |
| 流动相 | ||
| 溶剂 A 和 B | 纯水(缓冲液)/乙腈 | |
| 缓冲液 | 若有,水的缓冲液b(10–25 mM,pH2.5–3.0) | |
| %B | 10 min 内梯度 5%–100%a | |
| 流速 | 2.0 mL/mina | |
| 温度 | 30 °C 或 35 °C | |
| 样品 | ||
| 体积 | \(\leq\) 50 μL | |
| 重量 | \(\leq\) 10 μg | |
| \(k^*\)c | \(\approx\) 5 |
a:也可更换其他规格色谱柱,并使用下表推荐参数:
Table 4. Column volumes for various column configurations and recommended scouting gradient times
| L (mm) | dc (mm) | Vm (mL) | F (mL/min) | tG (min) | \(\Delta\phi\) |
|---|---|---|---|---|---|
| 250 | 4.6 | 2.5 | 1.0 | 60 | 90% |
| 150 | 4.6 | 1.6 | 2.0 | 20 | 90% |
| 150 | 2.1 | 0.33 | 0.4 | 20 | 90% |
| 100 | 4.6 | 1.0 | 2.0 | 10 | 90% |
| 100 | 2.1 | 0.22 | 0.4 | 10 | 90% |
| 50 | 2.1 | 0.11 | 0.5 | 5 | 90% |
对于不在表中的参数可用下式换算:
\[ k^*=\frac{0.87t_{G}F}{V_m\Delta\phi S} \]
- \(t_{G}\):梯度时间,min;
- \(F\):流速,mL/min;
- \(V_{m}\):为色谱柱的死体积,mL;
- \(\Delta\phi\):%B 梯度变化范围,如乙腈从 5% 线性升到 95%,\(\Delta\phi = 90\%\);
- \(S\):溶质敏感性常数(Solute Sensitivity Constant),用来描述溶质保留行为对流动相组成变化敏感程度的常数,对于小分子 \(S\) 大概在 4–5(常按 \(S \approx 4\) 估算),对于大分子 \(S\) 大概在 10–1000。
b:如 0.1% 的甲酸水溶液。
c:化合物在梯度洗脱过程中,从进入色谱柱到离开色谱柱,保留因子 \(k\) 是变化的,\(k^*\) 表示这段时间内 \(k\) 的平均值,\(k^*=\frac{0.87t_{G}F}{V_m\Delta\phi S}\)。
等度洗脱或梯度洗脱的选择
判断样品是否应该使用等度洗脱还是梯度洗脱:
\[ \Delta t_{R} = t_{-1} - t_1 \]
- \(t_{-1}\):最后一个目标峰的保留时间;
- \(t_1\):第一个目标峰的保留时间。
\(\frac{\Delta t_{R}}{t_{G}}\) 越小,表示全部色谱峰在某一浓度附近能够集中洗脱。
当 \(\frac{\Delta t_{R}}{t_{G}} \leq 0.25\):推荐使用等度洗脱;
当 \(\frac{\Delta t_{R}}{t_{G}} \geq 0.40\):推荐使用梯度洗脱。
对于 \(\frac{\Delta t_{R}}{t_{G}} \geq 0.10\),也可以直接考虑梯度洗脱。
等度洗脱方法开发
若使用等度洗脱,等度洗脱的初始 %B 可以由下式进行估计:
\[ \%B \approx \frac{100\Delta\phi}{t_{G}}(t_{avg} - t_{D}) - 2 \]
- \(t_{avg} = \frac{t_1 + t_{-1}}{2}\),即第一个目标峰和最后一个目标峰保留时间的均值。
- \(t_{D}\):滞留时间。
使用确定好的 %B 对方法进行验证,流程如下图:
graph TD A -- 是 --> B1 A -- 否 --> B2 A[1 < k < 10?] B1 -- 是 --> C1 B1 -- 否 --> C2 B1[Rs > 1.5?] C1["验证其余系统适用性项"] --> D1["结束,进行方法学验证"] C2["改变其他条件(如 pH、温度等)"] -.-> A B2["调整 %B"] B2 -.-> A
如何调整 %B
调整合适的流动相比例,使 \(1<k<10\),按下式估算需要调节的比例:
\[ logk=logk_w-S\phi \]
- \(k\):保留因子。
- \(logk\):保留因子的对数。
- \(logk_w\):当流动相为 100% 水相时,该化合物的保留因子的对数,为理论值。
- \(\phi\) :流动相中有机相的体积分数。例如,如果流动相是 70% 甲醇和 30% 水,那么 \(\phi=0.7\)。
- \(S\):溶质敏感性常数(Solute Sensitivity Constant),用来描述溶质保留行为对流动相组成变化敏感程度的常数,对于小分子 \(S\) 大概在 4–5(常按 \(S \approx 4\) 估算),对于大分子 \(S\) 大概在 10–1000。
梯度洗脱方法开发
优化保留因子 \(k^*\)
\[ k^*=\frac{0.87t_{G}F}{V_m\Delta\phi S} \]
- \(t_{G}\):梯度时间,min;
- \(F\):流速,mL/min;
- \(V_{m}\):为色谱柱的死体积,mL;
- \(\Delta\phi\):%B 梯度变化范围,如乙腈从 5% 线性升到 95%,\(\Delta\phi = 90\%\);
- \(S\):溶质敏感性常数(Solute Sensitivity Constant),用来描述溶质保留行为对流动相组成变化敏感程度的常数,对于小分子 \(S\) 大概在 4–5(常按 \(S \approx 4\) 估算),对于大分子 \(S\) 大概在 10–1000。
对于大多数的小分子样品(分子量 < 1000 Da)来说,Table 3 内推荐的其实梯度条件一般能够使他们的 \(k^*\) 平均值达到 \(\approx 5\),因此通常无需再考虑优化 \(k^*\)。
优化梯度选择性 \(\alpha^*\)
越来越多的证据表明,在起始的方法试验中,梯度时间和温度是调整 \(\alpha\) 的首选变量,因此常对他们首先进行改变(同时保持 \(0.5 \leq k^* \leq 20\))。
将梯度时间变为原来的 2–3 倍,同时保持 \(0.5 \leq k^* \leq 20\)。
通过改变温度,如增加 20 °C,查看分离是否得到改善。
以甲醇代替乙腈。
考虑更换色谱柱。
考虑使用分段梯度(由于不同仪器间的 \(t_D\) 不同,可能导致不同仪器间重现性差)
分析方法学开发流程
回顾样品信息
- 被分析物数量:需要分离多少色谱峰?
- 化合物化学结构(官能团)。
- 化合物的分子量。
- 化合物的 pKa。
- 化合物的 UV 光谱。
- 样品基质的性质:溶剂、填充物等。
- 化合物在有关样品中的浓度范围和定量要求。
- 样品的溶解度。
- 样品需要预处理吗?
- 流动相需要缓冲吗?
明确分离目的
- 主要目的是分析还是回收样品组分?
- 是否已知样品所有成分的化学特性,或是否需定性分析?
- 是否有必要解析出样品的所有成分(比如对映体、非对映体、同系物、低聚物、痕量杂质)?
- 如需定量分析,需精密度多高?
- 本法需用于几种样品剂型(原料、制剂、环境样品等)?需要一种以上的 HPLC 方法吗?
- 本法将仅用于分析几种样品,还是许多种?
- 将使用最终方法的常规实验室中,已有哪些 HPLC 设备和技术?
运行起始分离条件
- 按照 Table 3 中信息运行初始条件。
- 有出现什么问题吗?
- 可以使用等度分离吗?
优化梯度的保留因子 \(k^*\)(Table 3 内推荐的其实梯度条件一般能够使他们的 \(k^*\) 平均值达到 \(\approx 5\),因此通常无需再考虑优化 \(k^*\))
优化梯度选择性 \(\alpha^*\)
- 将梯度时间变为原来的 2–3 倍,同时保持 \(0.5 \leq k^* \leq 20\)。
- 通过改变温度,如增加 20 °C。
- 以甲醇代替乙腈重复步骤 1–4。
- 考虑更换色谱柱重复步骤 1–4。
- 考虑使用分段梯度。
调整梯度范围和形状
- 选择最佳的起始和最终的 %B,从而在分离度 \(R_s\) 合理的前提下实现最短的实验时间。
- 对于“较脏的”样品,加入坡度较大的梯度分段至 100% B。
- 加入梯度较大的梯度分段来加速色谱图后段的、间隔较宽的色谱峰的洗脱。
- 加入等度停留从而改善梯度前段洗脱出来的色谱法之间的分离度。
以步骤 5 或 6 中获得的最佳的分离效果为基础,平衡分离度和运行时间
测量连续的样品进样之间,色谱柱的必要平衡时间
注:平衡时间需要优化,建议从 \(2t_0\) 开始。
下图是一个梯度洗脱程序示例:
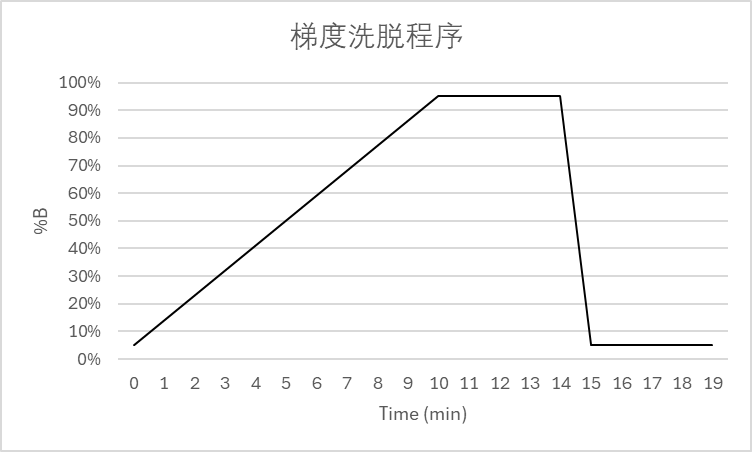
Figure 5. 梯度洗脱示例
Table 5. 梯度洗脱示例说明
| Time (min) | 说明 |
|---|---|
| 0–10 | 梯度洗脱 |
| 10–14 | 冲洗 |
| 14–15 | 将回到初始梯度浓度 |
| 15–19 | 平衡 |
References
斯奈德.实用高效液相色谱法的建立(第二版)[M].华文出版社,2001.
Lloyd R. Snyder, Joseph J. Kirkland, John W. Dolan. 现代液相色谱技术导论[M]. 人民卫生出版社, 2012.
“Making to the most of a Gradient Scouting Run” LCGC North America Vol. 31,Number 1, 2013.
HPLC Method Development- From Beginner to Expert, Part 1: https://www.agilent.com/cs/library/slidepresentation/public/method-development-101-from-beginner-to-expert-part-1-feb202024.pdf
液相色谱手册:https://www.agilent.com/cs/library/primers/public/5990-7595CHCN.pdf
液相分析方法开发工具书:https://www.waters.com/content/dam/waters/zh/library/brochures/2015/720008028zh.pdf